Znanstvenici Instituta Ruđer Bošković (IRB), poslijedoktorand dr. sc. Kruno Vukušić i voditeljica laboratorija prof. dr. sc. Iva Tolić, otkrili su mehanizam kojim stanice reguliraju trenutak pokretanja kromosoma prema središtu diobenog vretena, jednom od ključnih događaja stanične diobe, priopćeno je s IRB-a. Njihovo otkriće, koje je zbog širine rezultata Nature Communications objavio u dva zasebna članka, baca sasvim novo svjetlo na to kako stanice sprječavaju kobne pogreške u raspodjeli kromosoma.
tri vijesti o kojima se priča


Kako pojašnjavaju s IRB-a, preciznije razumijevanje načina na koji stanica uspostavlja red i koji molekularni mehanizmi „daju zeleno svjetlo“ za pravilnu raspodjelu DNK važni su za razvoj novih dijagnostičkih pristupa, otkrivanje terapijskih meta te osmišljavanje strategija koje bi u budućnosti mogle spriječiti ili ispraviti pogreške povezane s nastankom bolesti, uključujući rak.
Dr. sc. Kruno Vukušić, priznat stručnjak u području stanične biologije i diobe, izveo je zahtjevne eksperimente tijekom svog poslijedoktorskog usavršavanja u međunarodnom okruženju ERC Synergy tima. Danas se priprema za osnivanje vlastite istraživačke grupe te surađuje sa znanstvenicima iz Nizozemske, SAD-a, Njemačke i Švicarske, s kojima objavljuje radove u uglednim znanstvenim časopisima u sklopu projekata vrijednih više milijuna eura. Njegov ostanak i rad u Hrvatskoj na Institutu Ruđer Bošković važan je doprinos dugoročnom razvoju te jačanju međunarodne prepoznatljivosti domaće znanosti.
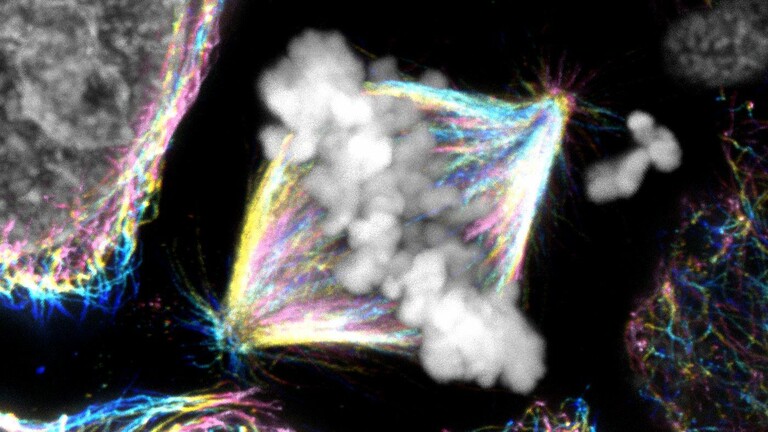
Naši rezultati pokazuju da protein CENP-E, ključan molekularni igrač u ranim stadijima stanične diobe, nije mehanički motor koji dovlači kromosome u središte stanice, kako se dugo vjerovalo, nego ključni regulator u stabilizaciji njihovih početnih vezanja na mikrotubule, ističe dr. sc. Vukušić, prvi autor rada. Bez te stabilizacije kromosomi ostaju blokirani, a pogreške u njihovoj raspodjeli izravno su povezane s nastankom tumora i drugih bolesti.
Prometna špica u svakoj stanici
Zamislite promet u najvećem mogućem gradu. Milijarde različitih vozila, milijarde križanja, milijarde uputa. Svaka vožnja mora završiti bez sudara, bez kašnjenja, bez greške. Baš takav grad postoji u nama i to u svakoj našoj stanici.
Svaka dioba stanice nalikuje prometnoj špici u velegradu. U toj slici kromosomi su vlakovi puni DNK-a, a mikrotubuli njihova složena prometna mreža, odnosno tračnice koje vode prema središtu stanice. Ako se samo jedan vlak pogrešno priključi ili zakasni, cijeli prometni sustav se urušava, što u slučaju stanice može na razini organizma dovesti do razvojnih anomalija, genetskih bolesti ili raka.
Kako stanica uspijeva održati red u toj gužvi? Odgovor na to pitanje ovih je dana došao iz Zagreba, s Instituta Ruđer Bošković. Dr. Kruno Vukušić i dr. Iva Tolić otkrivaju kako stanice izbjegavaju kobne pogreške prilikom prijenosa DNK na iduću generaciju. U tom procesu ključnu ulogu igra protein CENP-E, ali ne onako kako se do danas smatralo.

Semafori koji blokiraju promet
Da bismo shvatili ulogu proteina CENP-E, zamislimo veliki željeznički kolodvor. Na peronu se skupljaju vlakovi, u našem slučaju to su kromosomi koji nose pakete DNK-a. Svi moraju stići na glavni kolosijek u sredini stanice koristeći tračnicu točno određenog tipa i smjera. Ako neki vlak zakasni ili promaši spojnicu, raspodjela DNK ide po zlu, s ozbiljnim posljedicama poput razvoja genetskih poremećaja ili raka.
Dugo se vjerovalo da je CENP-E lokomotiva koja vuče zaostale vagone prema centru. No znanstvenici IRB-a sada su pokazali da je istina drukčija. Protein CENP-E nije vučni motor, nego glavni inženjer. Njegov je zadatak osigurati da se naš vlak kromosoma uopće može pravilno zakvačiti na tračnice odnosno mikrotubule unutar stanice. Tek kad je spojnica sigurna, vlak može krenuti i doći do središta, gdje ga čeka daljnja raspodjela.
Ali tu priča ne staje.
Zašto kromosomi često zapnu kada nema glavnog inženjera? Jer proteini koji upravljaju prometom, a koji djeluju na ključnim dijelovima mreže, poznati pod nazivom Aurora kinaze, funkcioniraju poput sigurnosnog semafora. To znači da pale crveno svjetlo kada uvjeti za kretanje kromosoma nisu ispunjeni. Protein CENP-E tada intervenira i osigurava da semafor prebaci na zeleno u pravom trenutku i na pravom mjestu. Znači, protein ne vuče kromosome u središte stanice, nego im omogućuje da sigurno krenu.
Redefiniranje uloga nakon dva desetljeća
Ova otkrića mijenjaju gotovo dvadeset godina stari model. Umjesto da djeluje prvenstveno kao motor, CENP-E se pokazao ključnim regulatorom početne faze poravnanja kromosoma. Novi model bolje objašnjava kako stanica koordinira precizan razmještaj DNK, što je temelj uredne diobe.
Ovim istraživanjem predložili smo ujedinjeni model u kojemu je poravnanje kromosoma neodvojivo povezano s biorijentacijom, objašnjava prof. dr. sc. Tolić. Drugim riječima, protein CENP-E omogućuje početak pravilnog poravnanja time što modulira aktivnost Aurora kinaza i stvara uvjete za stabilno vezanje kromosoma. To je temeljna promjena u načinu na koji objašnjavamo dinamiku diobe stanica.
Profesorica Tolić međunarodno je priznata biologinja i voditeljica Laboratorija za biofiziku stanice na IRB-u. Autorica je više od 100 radova objavljenih u najuglednijim znanstvenim časopisima, dobitnica je dvaju prestižnih projekata Europskog istraživačkog vijeća (ERC), često nazivanih 'znanstvenim Oscarima', te brojnih priznanja, uključujući nagradu Ignaz Lieben. Vodeća je znanstvenica u području stanične diobe, a članica je i EMBO-a i Academia Europaea te članica suradnica HAZU.
Potpora Europe i nacionalna infrastruktura
Istraživanje je rezultat višegodišnjeg rada uz snažnu međunarodnu i nacionalnu podršku, uključujući prestižni ERC, Hrvatsku zakladu za znanost, bilateralne projekte te ulaganja Vlade RH i EU kroz Europski fond za regionalni razvoj. Ključnu ulogu imala je i infrastruktura Sveučilišnog računskog centra (Srce), čija je tehnološka podrška omogućila provođenje složenih analiza i simulacija.
Na lokalnoj adresi, ali s globalnim značajem, tim s IRB-a rasvijetlio je ključnu ulogu proteina CENP-E u diobi kromosoma, pridonoseći redefiniranju modela stanične diobe u svjetskoj znanosti.
Učeći kako ti mikroskopski proteini i njihovi regulatori međusobno djeluju, približavamo se razumijevanju, a u budućnosti i potencijalnom ispravljanju onoga što u bolesti krene po zlu, zaključuju dr. sc Kruno Vukušić i prof. dr. sc. Iva Tolić.